Группа американских ученых выяснила, что рак поджелудочной железы способен перепрограммировать себя и изменять метаболизм, чтобы распространиться на другие ткани и органы и стать невосприимчивым к химиотерапии. В то же время исследователи обнаружили и его ахиллесову пяту: для метастазирования ему необходима глюкоза. «Лента.ру» рассказывает о деталях исследования, опубликованного в журнале Nature.
Несмотря на значительные успехи в лечении раковых опухолей, некоторые виды рака остаются высоколетальными. Например, протоковая аденокарцинома поджелудочной железы, занимающая в развитых странах второе место по количеству смертей от злокачественных новообразований. Ее смертоносность объясняется тем, что первичная опухоль состоит из различных популяций клеток, которые отличаются друг от друга генетическими, эпигенетическими и другими признаками. Подобрать правильные лекарственные препараты очень трудно: некоторые клетки могут оказаться невосприимчивыми к лечению.
Кроме того, внутри раковой опухоли происходят эволюционные процессы, и одни субпопуляции, возникшие, например, в результате мутаций, получают преимущество над другими. Тем не менее было показано, что даже отличающиеся друг от друга раковые клетки содержат одинаковые драйверные мутации, способствующие росту злокачественных новообразований. К тому же подавляющее большинство (если не все) уникальных для каждой субпопуляции мутаций, как выяснилось, — «автостопщики». То есть они никак не влияют на способность клеток размножаться, но распространяются из-за того, что находятся рядом с драйверной мутацией.
Возникает вопрос: что же приводит к возникновению гетерогенных опухолей и образованию невосприимчивых к лекарственным препаратам метастазов? По мнению исследователей, дело не в генетических мутациях, а в эпигенетической регуляции. В результате присоединения различных молекул к ДНК одни гены выключаются, а другие усиливают свою активность. Эти изменения могут передаваться от родительской клетки дочерним, что в конце концов формирует субпопуляцию. Чтобы выяснить, как это происходит, ученые изучили изменения в эпигеноме (общем эпигенетическом состоянии клеток) в процессе формирования субпопуляций и метастазов аденокарциномы поджелудочной железы.
Использовались образцы тканей из первичных и вторичных опухолей пяти пациентов. Взяли различные субпопуляции, в том числе и ту, от которой произошли все остальные (именно она вызвала рак, а ее потомки выступили «семенами» для метастаз). Затем был проведен иммуногистохимический анализ: с помощью помеченных антител выявлялись сцепленные с ДНК белки (гистоны), к которым присоединены две или три метильные группы (СН3). Метилирование — один из способов эпигенетической регуляции, способной как подавлять активность генов, так и усиливать ее. Эффект зависит от того, к какому типу гистона и в каком его месте присоединена СН3. Ученых интересовало метилирование гистона H3 в сайте К9, которое, как показано, приводит к ингибированию гена, связанного с белком.

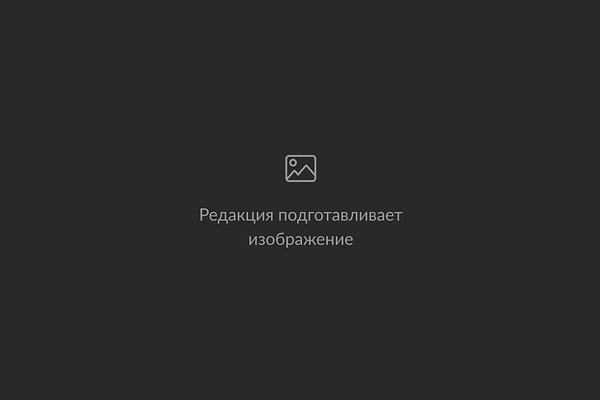
Печень с метастазами, распространившимися от рака поджелудочной железы
Фото: Haymanj / Wikipedia
Исследователи выявили степень эпигенетических изменений во всех гистонах H3, располагающихся в компактной области хромосом — гетерохроматине. Это плотно свернутые участки хромосом, где гены малоактивны. Однако ученых интересовал не весь гетерохроматин, а его отдельные области (домены) — LOCK и большие гипометилированные ДНК-блоки. LOCK обычно характеризуются высоким уровнем метилирования H3, а гипометилированные блоки в раковых опухолях — невысоким. Оказалось, что у пациентов, у которых опухоль метастазировала в печень и легкие, уровень метилирования гистонов был низким. У тех больных, чьи метастазы ограничились лишь брюшной областью, число модифицированных гистонов оставалось высоким.
Это говорит о том, что вторичные опухоли образуются из-за того, что отдельные субпопуляции злокачественных клеток перепрограммируют себя, активируя те гены, которые должны «молчать». Дополнительные анализы с клеточными линиями, извлеченными из метастазов и первичных опухолей восьми пациентов, подтвердили, что развитие рака сопряжено с глобальной перестройкой эпигенома.

Микрография протоковой аденокарциномы поджелудочной железы
Изображение: KGH / Wikipedia
Изменения были также обнаружены и в эухроматине — активной и некомпактной области генома. Одни гены, находящиеся тут, активируются из-за обогащения метильными группами сайта K36 у гистонов H3. Другие, наоборот, подавлялись из-за падения уровня метилирования K36.
Ученые проанализировали, какие именно гены были затронуты эпигенетическими изменениями, чтобы выяснить, действительно ли перепрограммирование связано с агрессивностью опухолей. Установлено, что в области LOCK при падении уровня метилирования активируются гены, связанные с деятельностью оксидоредуктазы. Этот фермент является антиоксидантом и обезвреживает активные формы кислорода, что делает клетки устойчивыми к окислительному стрессу. В эухроматине активируются гены, участвующие в восстановлении ДНК, и опухоли приобретают устойчивость к химиотерапии.
Как препятствовать росту опухоли поджелудочной железы? Установлено, что клетки метастазов поглощают много глюкозы, которая усиливает синтез различных веществ, а также ослабляет генерацию активных форм кислорода, помогающих подавлять рост рака. Кроме того, пентозофосфатный путь (альтернативный способ окисления глюкозы) связан с эпигенетической регуляцией, способствующей росту опухоли. Он может быть потенциальной целью для лекарственных препаратов, предотвращающих метастазы аденокарциномы поджелудочной железы.